| GLI ANELLI ILLUSTRATI DAL DOTT. ALESSANDRO MULARONI |
 |
 |
 |
|
ANELLI INTRASTROMALI
Abbiamo il piacere di ospitare in questo numero dell’Oculista Italiano, nella rubrica dedicata alla chirurgia rifrattiva, il Dott. Alessandro Mularoni, oculista dirigente medico dell’Ospedale Maggiore di Bologna, il quale si occupa di chirurgia del segmento anteriore (cataratta, glaucoma, cheratoplastica) ed in particolare di chirurgia refrattiva. Tra i suoi meriti va annoverato il fatto che è stato uno dei pionieri in Italia e nel mondo nell’utilizzo dell’ablazione customizzata iniziando fin dal 1997. Ha una vastissima esperienza in campo di anelli intrastromali per la chirurgia della miopia, cheratocono, e per i ritrattamenti in esiti di chirurgia rifrattiva. Proprio in virtù della sua ampia esperienza e vasta conoscenza delle problematiche relative abbiamo pensato di realizzare un articolo-intervista sull’utilizzo degli anelli intrastromali, tema di grande attualità nel campo della chirurgia rifrattiva e corneale avvalendoci della sua preziosa collaborazione, per la quale lo ringraziamo. In forma semplice, comprensibile anche ai non addetti ai lavori della ultraspecialistica branca della chirurgia rifrattiva implantologica, ma allo stesso tempo esauriente ed aggiornata, il Dott. Mularoni illustrerà la sua esperienza, ed esporrà il suo parere, in risposta alle domande che, ritengo, pongono l’accento sui principali punti fermi ed ancora da risolvere in questo interessante ed innovativo settore della chirurgia corneale rifrattiva. Leonardo Mastropasqua
Che cosa sono gli anelli intrastromali e quali sono le loro applicazioni?
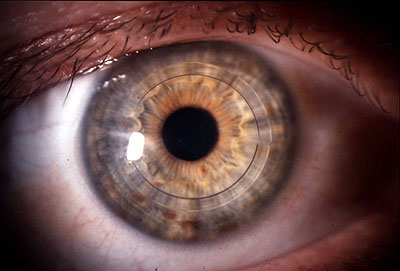
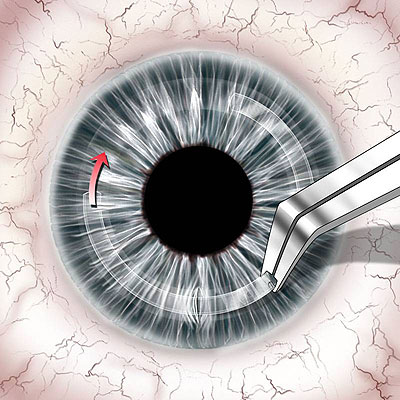
Gli anelli intrastromali o ICR o INTACS rappresentano un valido strumento per il chirurgo refrattivo con possibilità applicative in continua evoluzione. Oltre alla correzione della miopia lieve, vengono impiegati in pazienti con cheratocono ed in pazienti già sottoposti a chirurgia refrattiva al fine di migliorare risultati non soddisfacenti. Posizionati nello stroma periferico, a circa 2/3 dello spessore, con un traumatismo minimo, inducono una variazione della superficie anteriore mantenendo l’asfericità positiva della cornea. Essi risparmiano la zona ottica e preservano le opzioni refrattive future del paziente, in quanto l’intervento ha le caratteristiche della rimovibilità. Progettati nel 1978 da Gene Reynolds come anello unico di 360°, hanno subito varie evoluzioni fino ad assumere la conformazione attuale. Dopo una fase sperimentale, l’FDA nel 1999 ha approvato l’utilizzo degli Intacs per miopie comprese fra 1 e 3 diottrie. La protesi, attualmente prodotta da Addition Technology, si compone di 2 semi-anelli in polimetilmetacrilato (PMMA), ultrasottili e trasparenti con un bordo esagonale, aventi ciascuno una lunghezza d’arco di 150° (Fig. 1). Quando impiantati il diametro esterno misura 8,1 mm, mentre quello interno 6,8 mm; ad una estremità è presente un foro di 0,28 mm di diametro, che facilita la manipolazione da parte dell’operatore.
Fig. 1: Immagine di 2 segmenti impiantati superiormente ed inferiormente in un paziente con cheratocono.
Qual è il loro meccanismo di azione?
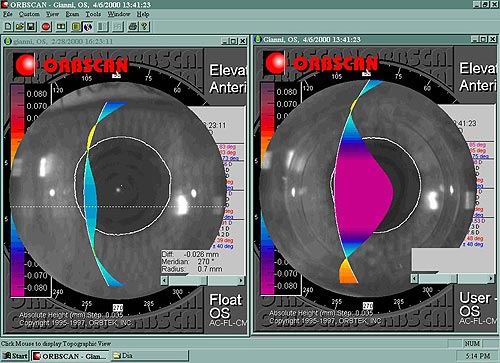
Gli ICR sono elementi rigidi occupanti spazio che modificano la lunghezza d’arco della curvatura anteriore della cornea con un’azione meccanica. Poiché le lamelle corneali sono formate da fibre continue che corrono da limbus a limbus, posizionando questi dispositivi alla periferia corneale si verifica una separazione delle lamelle con conseguente accorciamento della lunghezza dell’arco corneale anteriore. Il risultato è un appiattimento corneale dalla periferia verso il centro proporzionale allo spessore dell’impianto, dal momento che l’aumento di spessore dell’anello aumenta lo spazio che si crea tra lamella e lamella. L’utilizzo di sistemi topografici con studio altitudinale, ha permesso di chiarire più in dettaglio i cambiamenti meccanici indotti dagli Intacs sia sulla superficie anteriore della cornea, sia sulla superficie posteriore (Fig. 2). Nella sede d’impianto dell’anello si evidenzia un’espansione della superficie corneale a cui fa seguito un appiattimento nella zona corneale centrale. L’azione refrattiva degli anelli si esplica determinando un cambiamento nella lunghezza focale dell’occhio senza, però, eliminare l’asfericità corneale fisiologica. Questa infatti è responsabile della buona risoluzione del nostro sistema visivo eliminando le cosiddette aberrazioni sferiche. La perdita della asfericità positiva della cornea indotta da altre procedure come la cheratotomia radiale o la fotocheratectomia refrattiva induce i noti fenomeni di aberrazione dell’immagine tipica delle forme oblate.
Fig. 2: Studio profilometrico pre e post-operatorio di un paziente con miopia residua dopo LASIK.
Perché impiantare a 2/3 dello spessore corneale? La profondità dell’impianto, localizzata al 68% dello spessore corneale, è definita da due ordini di fattori: da un lato la necessità di preservare l’integrità della membrana di Bowman e della membrana di Descemet, dall’altro di usufruire della scarsa reattività dello stroma. Si è visto che impianti più superficiali possono determinare problemi di trofismo corneale con “melting” ed estrusione dell’anello, impianti più profondi superiori all’80% dello spessore corneale, non hanno effetto refrattivo in quanto provocano una deformazione corneale con spostamento in avanti della superficie corneale posteriore.
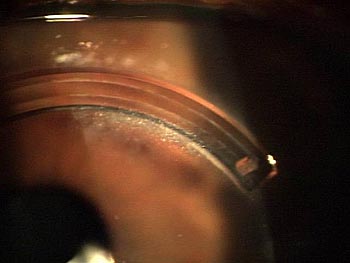
E riguardo alla biocompatibilità? Impianti intracorneali per variare il potere refrattivo della cornea sono allo studio da molti anni. Alcuni materiali (polisulfone, silicone, idrossimetilmetacrilato) sono stati abbandonati per la loro scarsa biocompatibilità o perché poco adatti ad indurre modificazioni rifrattive ad alta precisione. Il PMMA si è invece dimostrato idoneo sotto entrambi gli aspetti. Infatti dopo l’impianto d’ICRS si verificano i cambiamenti rifrattivi desiderati, mentre le reazioni del tessuto corneale non interessano la zona ottica e non compromettono il trofismo del tessuto stesso. Fra queste segnaliamo: ► l’haze corneale periferico, che si manifesta a livello dei canali intrastromali nell’immediato periodo postoperatorio per separazione meccanica delle lamelle stromali creata dalla manovra chirurgica. ► depositi nelle aree d’incisione dei canali intrastromali: compaiono intorno al 2° mese, hanno dimensioni inferiori a 0,2 mm di diametro e possono presentarsi con un aspetto cristallino e rifrangente oppure essere bianco-calcarei e confluire tra loro. Sulla loro origine sono state fatte varie ipotesi (Fig. 3). ► opacità gelatinose: presenti intorno all’8° mese successivo l’impianto, sono formate da cheratociti circondati da strati concentrici di collagene di nuova sintesi e da proteoglicani (studio al microscopio elettronico). ► depositi epiteliali ferrosi, a forma di semiluna, si dispongono a circa 1 mm dal margine interno degli anelli a livello dell’emicornea inferiore, lungo i meridiani che decorrono approssimativamente dalle ore 3 alle ore 9. La loro formazione è dovuta all’evaporazione del film lacrimale che determina un aumento della concentrazione del ferro in soluzione con aumentato up-take del ferro da parte delle cellule epiteliali e da un ridotto ricambio delle cellule superficiali in quella zona.
Fig. 3: A 7 mesi dall’intervento, sono visibili lungo il bordo interno dell’anello depositi biancastri e rifrangenti di piccole dimensioni. È bene ricordare che tutte queste manifestazioni non determinano alterazioni visive verificandosi al di fuori dell’asse visivo centrale e si autolimitano nel tempo. Gli studi effettuati sull’endotelio corneale con misurazioni in cornea centrale e periferica, a 24 mesi dopo l’impianto, non hanno evidenziato diminuzioni significative nel numero ed alterazioni nella forma delle cellule endoteliali.
Quali sono la tecnica e lo strumentario chirurgico utilizzati?
Per questo intervento esiste un set di strumenti specifici che comprende: ► un marcatore per posizionamento dell’incisione e dei dissettori: è costituito da un cilindro alla cui estremità un reticolo di centratura permette di allineare l’incisione radiale e la conseguente posizione dei segmenti rispetto al centro corneale, in precedenza individuato con una marcatura. Tale strumento viene inoltre utilizzato per posizionare opportunamente la guida di centratura e suzione, in una fase successiva della procedura chirurgica. ► Pocketing hook, pocketing lever, spreader o delaminatore stromale (da 3 mm): tre strumenti per la formazione del tunnel e per le manovre di slamellamento della cornea. ► Unità di suzione con guide e dissettori per la formazione dei canali (manovra che viene eseguita con il bulbo in suzione per prevenire possibili rotazioni durante la dissezione). ► Pinza per anelli: questa apposita pinza in titanio è caratterizzata da una scanalatura terminale che si adatta esattamente alla configurazione dell’anello e permette una facile estrazione dall’astuccio porta-protesi, una presa sicura dell’impianto ed un agevole inserimento di ciascun semianello nel canale stromale.
Tecnica chirurgica
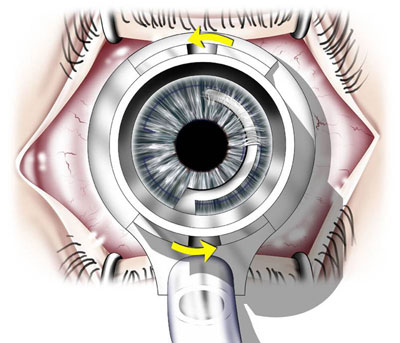
Nella fase preoperatoria il cul di sacco congiuntivale viene disinfettato con iodio-povidone al 2,5%. Si posiziona il telo come nell’intervento di cataratta, facendo attenzione ad isolare bene le ciglia con il blefarostato. Può essere utile servirsi di telini sterili adesivi per isolare le ciglia e di un telo adesivo con foro già preparato come nelle procedure lasik. Generalmente la procedura viene eseguita in anestesia topica mediante l’instillazione di gocce di ossibuprocaina cominciando dieci minuti prima dell’intervento. In caso di pazienti agitati o scarsamente collaboranti si può procedere ad una anestesia loco-regionale ed alla sedazione. È sempre consigliabile utilizzare guanti privi di talco, come in ogni procedura di chirurgia refrattiva. Vengono marcati il centro corneale geometrico, la sede dell’incisione radiale e la posizione in cui si impianteranno gli anelli. Si procede alla pachimetria intraoperatoria ed al settaggio del bisturi di diamante al 68% dello spessore corneale; si effettua un’incisione di 1,8 mm (da 1,2 a 2 mm) in direzione radiale, lasciando almeno 1 mm di distanza dal limbus. Con gli strumenti precedentemente descritti si creano le due tasche, destra e sinistra, alla stessa profondità. In questa fase si può usare uno strumento con parte terminale a “T” (Rosen-Propeller) per costruire le tasche sullo stesso piano, dal momento che si procede contemporaneamente su entrambi i lati dell’incisione. Dopo aver anestetizzato con una microsponge ad anello la congiuntiva ed il limbus, si posiziona la guida collegata alla pompa del vuoto e si applica una suzione, inizialmente di 400-500 mBar e successivamente fino a 600 –670 mBar. È importante non superare i 750 mBar in quanto si potrebbero verificare emorragie congiuntivali e retiniche. Se si perde la suzione dopo aver creato un vuoto superiore a 500 mBar per diversi secondi, è bene aspettare 5 minuti prima di riavviare la procedura affinché si ristabilisca la normale perfusione vascolare oculare. Con il bulbo in suzione si creano i tunnel corneali ruotando i due dissettori in senso orario e antiorario (Fig. 4). La formazione del tunnel va continuamente monitorata tenendo conto delle variazioni di resistenza: se diminuisce potrebbe essere un segno di tunnel troppo superficiale o di perforazione, se aumenta di andamento non parallelo alle lamelle stromali. A questo punto l’anello intrastromale viene afferrato con le apposite pinze dall’astuccio ed inserito direttamente attraverso l’incisione dentro il tunnel stromale; una volta inserita la prima metà, viene afferrato a circa metà della porzione ancora esterna e completata l’inserzione (Fig. 5).
Fig. 4: Creazione del tunnel stromale mediante dissettore anti-orario con bulbo mantenuto in suzione.
Fig. 5: Manovra di inserimento dell’anello all’interno del tunnel mediante apposita pinza “Cortesia del Dott. C.F. Lovisolo”
I segmenti non dovrebbero mai toccare la superficie della cornea o la congiuntiva, ma essere presi dall’apposito astuccio ed essere immessi direttamente all’interno del canale, evitando così eventuali contaminazioni. Si sutura infine l’incisione con 1 o 2 punti in nylon 10/0, cercando di ottenere l’apposizione dei margini poiché un’incisione non suturata tende ad aprirsi per l’azione meccanica di stiramento degli anelli e favorisce la penetrazione di cellule e batteri; una sutura troppo stretta può indurre astigmatismo. Si prescrive una copertura antibiotica ad ampio spettro, in collirio, da utilizzare 4 volte al dì per i primi 15 gg ed analgesici al bisogno.
Quando utilizzare gli anelli nella correzione della miopia?
Dal 1997 al 1999 abbiamo impiantato 20 pazienti con miopia compresa fra 1 e 5 diottrie ottenendo buoni risultati; tuttavia la tecnica garantisce una minor precisione rispetto alla PRK, per cui attualmente la riserviamo solo a pazienti miopi con cornee sottili o con sospetta o accertata ectasia della superficie posteriore. La correzione della miopia mediante l’impianto di ICR rappresenta sicuramente la procedura più praticata e con follow-up più lungo. Il differente spessore degli anelli (da 0,25 a 0,45 mm con incrementi di 0,05 mm) permette la correzione di miopie in un range compreso fra 1 e 4,5 diottrie. Negli Stati Uniti è stato effettuato uno studio multicentrico comprendente 450 pazienti, suddiviso in varie fasi, per verificare l’efficacia, la predittività, la sicurezza e la stabilità della procedura in occhi miopi con miopia compresa fra 1 e 6 diottrie. Questo studio si è concluso con risultati a lungo termine estremamente incoraggianti e nel 1999 l’FDA ha approvato l’utilizzo di questi dispositivi per la correzione di miopie comprese fra 1 e 3 diottrie. Come detto, in questa fascia di miopia, questa tecnica entra in competizione con la PRK, rispetto alla quale presenta due principali limitazioni: può correggere solo miopie medio-basse e con astigmatismo inferiore ad una diottria; gli anelli a disposizione hanno step di 0,05 mm (50 micron) e quindi la correzione non può essere precisa come nella PRK. Fra i vantaggi, oltre al fatto che la zona ottica centrale rimane risparmiata e l’intervento ha le caratteristiche della aggiustabilità e della rimovibilità, va ricordata l’estrema rapidità del recupero visivo (nello studio riportato da Schanzlin il 33% dei pazienti in prima giornata aveva un visus di 10/10, il 13% di 12/10). Inoltre è l’unica tecnica al momento che ha realmente dimostrato di poter raggiungere la cosiddetta supervisione: nello studio di Schanzlin a 2 anni dall’intervento il 76% dei pazienti presentava un visus naturale di 10/10, il 55% di 12/10, nel 21% dei casi era 16/10. Questo grazie al fatto che si mantiene la fisiologica prolatura della cornea o meglio si induce una pseudoprolatura capace di determinare un’ottima prestazione visiva.
Quali sono i cheratoconi che possono beneficiare dell’impianto di anelli intrastromali?
L’idea di utilizzare gli ICR nella terapia del cheratocono nasce dalle limitazioni delle tecniche chirurgiche attualmente utilizzate e dal desiderio di utilizzare interventi conservativi in soggetti giovani e con endotelio solitamente in ottimo stato. L’impianto di ICR nel cheratocono rappresenta al momento la tecnica più conservativa in quanto si lavora sul tessuto del paziente per indurre una modificazione di forma; per questo rappresenta una tecnica con finalità soprattutto rifrattive. Da un lato si hanno i vantaggi della tecnica scarsamente invasiva con basso rischio di complicanze chirurgiche e con mantenimento del proprio endotelio e dei propri tessuti, dall’altro lo svantaggio di mantenere un tessuto patologico e refrattivamente irregolare come quello del cheratocono. Da questo derivano una serie di limitazioni nella selezione dei pazienti; vanno operati: a) cheratoconi con trasparenza della cornea centrale e spessore pachimetrico minimo nella zona di impianto degli anelli di 400m. b) pazienti con intolleranza alle lenti a contatto. c) coni con K medio misurato nei 5-6 mm centrali inferiore a 53 diottrie ed ectasia periferica. I nostri risultati, relativi a più di 100 casi, e concordi con quelli presenti in letteratura (Colin 2002, Siganos 2003) hanno evidenziato: un miglioramento dell’acuità visiva naturale, un miglioramento dell’acuità visiva corretta, riduzione dei valori cheratometrici e dell’area di estensione del cheratocono, aumento della regolarità topografica della regione centrale. Al momento stiamo studiando una serie di indici topografici pre e postoperatori per una valutazione dell’efficacia dell’intervento e dei criteri di selezione del paziente. Difficile al momento valutare se l’impianto abbia anche un’azione contenitiva sulla progressione della patologia ectasica, mentre è significativo il fatto che nei casi in cui gli anelli sono stati espiantati ed è stato effettuato un trapianto di cornea il decorso postoperatorio è stato regolare (Siganos 2003). La procedura chirurgica è quella standard; è importante fare un’attenta valutazione pachimetrica delle varie aree corneali poiché si agisce su un tessuto assottigliato ed ectasico.
Attualmente l’utilizzo più innovativo e promettente di questi dispositivi sembra essere nei postumi di chirurgia rifrattiva; qual è la tua esperienza?
Pazienti già sottoposti a chirurgia rifrattiva e che hanno ottenuto risultati non soddisfacenti o comunque migliorabili rappresentano sicuramente l’ultima e più interessante indicazione all’uso di questi dispositivi. La mia esperienza riguarda sia pazienti sottoposti a chirurgia laser, cioè prk e lasik, sia pazienti operati con chirurgia incisionale: ► miopie residue in esiti di lasik: possono derivare da ipocorrezioni non programmate, da regressione e da ipocorrezioni desiderate in cui lo spessore residuo sotto il lembo sconsiglia un’ulteriore ablazione. In questi casi abbiamo utilizzato anelli di ugual spessore seguendo il nomogramma per la miopia. L’incisione è stata posta ad ore XII in caso di hinge superiore e temporale in caso di hinge nasale. La nostra esperienza relativa a 15 casi con follow-up minimo di 14 mesi ha evidenziato ottimi risultati: l’UCVA è migliorata nel 100% dei casi, nessun paziente ha perduto linee di acuità visiva corretta, il 70 % dei casi presentava un equivalente sferico a 14 mesi compreso fra ± O.50 diottrie dalla correzione desiderata. Questo studio ha inoltre mostrato una riduzione significativa dell’aberrazione sferica pre impianto di ICR e miglioramenti soggettivi molto evidenti. ► decentramenti post-lasik o post-prk, non correggibili con tecniche di ablazione customizzata o con altre tecniche per mancanza di spessore corneale; li abbiamo trattati con impianto di anelli di differente spessore nelle due emicornee: la sede dell’incisione si decide in base all’asse del decentramento. ► disturbi visivi legati a zone ottiche piccole in esiti di lasik in pazienti miopi elevati con spessore corneale residuo inferiore a 250 micron; possono essere trattati con segmenti intrastromali: si ottiene un allargamento significativo della zona ottica che determina un netto miglioramento dei disturbi soggettivi pre-operatori. ► sfiancamenti ed ectasia post-lasik possono giovarsi dell’impianto di anelli nella riduzione dell’astigmatismo irregolare e della miopia indotta solo ectasie non avanzate (Alio 2002, Lovisolo 2002, Kymionis 2003) ► irregolarità e sfiancamenti post-cheratotomia radiale, abbiamo trattato alcuni casi con astigmatismo elevato ed irregolare con ottimi risultati; tuttavia esistono importanti difficoltà chirurgiche con possibili complicanze intraoperatorie, quali apertura delle incisioni radiali o della camera anteriore che possono rendere imprevedibili i risultati. ► corneal bioptic alcuni autori propongono nelle ametropie elevate di tipo miopico, di effettuare un flap corneale, un impianto di segmenti intrastromali dopo alcuni mesi e successivamente, a refrazione stabilizzata, riaprire il lembo e trattare il difetto rimasto.
È opinione comune che l’intervento abbia le caratteristiche della reversibilità, ma questo è reale?
No, non è una tecnica reversibile poiché da un punto di vista anatomico abbiamo creato due tunnel intrastromali e modificato i rapporti fra le lamelle; ma ha le caratteristiche della rimovibilità, poiché una volta rimosse le protesi, sia da un punto di vista rifrattivo sia da un punto di vista topografico si torna alla situazione pre-operatoria (Chan 2001, Gomez 2000); inoltre la tecnica ha le caratteristiche della aggiustabilità; si possono rimuovere i segmenti in qualsiasi momento e sostituirli con altri di caratteristiche differenti. In quali situazioni è consigliabile rimuovere i segmenti? ► ipocorrezioni ed ipercorrezioni del difetto miopico. I segmenti in sede vengono sostituiti con altri di maggior o minor spessore; ► difetti epiteliali del tessuto sovrastante gli ICR. Impianti troppo superficiali associati ad eventuali difetti epiteliali e “melting” richiedono l’asportazione dell’anello ed il rinvio della procedura di 3 mesi. ► presbiopia. L’insorgenza della presbiopia in pazienti con riduzione dell’accomodazione trattati precedentemente con ICR per correzione di miopia, possono usufruire della reversibilità della procedura per entrambi gli occhi o in monovisione. L’intervento di rimozione si effettua in anestesia topica mediante riapertura dell’incisione presente con bisturi mono-uso. Si ricerca il piano della tasca corneale e mediante l’uncino di Sinskey si aggancia l’anello a livello del foro di posizionamento. Se necessario, l’anello viene sostituito e si completa con sutura dell’incisione.
Parliamo ora delle complicanze e della loro risoluzione
Si possono dividere complicanze intraoperatorie e post-operatorie. Le complicanze intraoperatorie riguardano l’errata esecuzione di tempi o manovre chirurgiche e come tali si inseriscono nella normale curva di apprendimento. Le complicanze postoperatorie si dividono in precoci (chemosi, emorragie sottocongiuntivali, edema corneale), che si verificano nei primi sette giorni dopo l’intervento e sono legate al trauma chirurgico ed alla flogosi che segue, e tardive. Queste ultime insorgono non prima della settima giornata. Fra le tardive ricordiamo: ► opacità (haze) e depositi corneali localizzati lungo i tunnel. Le opacità sono dovute alle manovre di separazione delle lamelle. I depositi, spesso frequenti (68 %) si localizzano lungo i canali e sono più frequenti e maggiori di diametro per i segmenti più spessi. ► infezioni: infiltrati a livello dell’incisione o del tunnel possono progredire sia lentamente sia rapidamente. Va prontamente instaurata una terapia antibiotica ad ampio spettro locale e generale; il decorso clinico può consigliare l’asportazione dell’anello se l’infezione è localizzata nella parte distale del canale e quindi non aggredibile con lavaggi di antibiotici. Nel trial clinico americano e nella nostra esperienza, si è verificato un caso di infezione da Staphilococcus epidermidis, normale saprofita del sacco congiuntivale. La prevenzione di questa complicanza si ottiene evitando contaminazioni del segmento durante l’impianto (contatto prolungato con congiuntiva e cornea), utilizzando una terapia antibiotica ad ampio spettro per i primi 15 gg postoperatori (fluorochinolonici ed aminoglicosidi) e mediante un’attenta monitorizzazione postoperatoria una volta sospesa questa terapia. - difetti epiteliali secondari ad un assottigliamento stromale per impianto troppo superficiale. ► astigmatismo indotto (spesso correggibile con lente corneale). ► ridotta sensibilità corneale. ► panno e neovascolarizzione. Si verificano con maggior frequenza in portatori di lenti a contatto ed in pazienti con panno già presente preoperatoriamente. Le cause possono essere le seguenti: a) incisione troppo vicino al limbus o in area limbare con neovasi o panno b) crescita epiteliale nell’incisione con introduzione di batteri o detriti che determinano una flogosi cronica. c) presenza di infezione-infiammazione di basso grado che non si manifesta finché non si sospende la terapia postoperatoria. d) bordo degli anelli troppo vicino all’incisione. I neovasi sono sensibili alla terapia corticosteroidea.
In base all’esperienza maturata in questi anni quali possono essere considerate i successi, gli insuccessi e quali le prospettive future di questi dispositivi?
La nostra esperienza è iniziata nel 1997 quando il dott. Tassinari ha impiantato i primi casi in Italia di pazienti con miopia lieve ed è proseguita allargando il campo di applicazione gradualmente a pazienti con cheratocono, esiti di chirurgia rifrattiva laser ed incisionale. Una esperienza così lunga ed ampia ci ha consentito con piccoli passi di migliorare tecnica chirurgica e soprattutto le indicazioni che al momento rappresentano il punto focale per avere un buon successo. Il futuro ed in parte già il presente si muovono verso la ‘customizzazione‘ dell’impianto così come sta accadendo per le altre branche della chirurgia rifrattiva: per strutture corneali normali la personalizzazione dell’intervento è molto vicina, per cornee patologiche mancano ancora importanti conoscenze sulla biomeccanica.
Fonte:
http://www.sifi.it/archivio/IT137/rubriche/rubri06.htm
|